近日,我室谢海燕教授团队在Cell Biomaterials杂志发表了题为“Deciphering endogenous CD8⁺ T cell interactions using an engineered sortase A system”的研究论文。该研究通过将工程化分选酶A(SrtA)与荧光能量转移(FRET)传感技术结合,建立了特异响应型体内邻近标记技术,原位精准解析了内源CD8⁺ T细胞与肿瘤细胞、胶原等的相互作用,可用于抗肿瘤药物疗效的预测。

肿瘤免疫疗法的快速发展正在重塑癌症治疗格局。其中,细胞毒性T淋巴细胞作为适应性免疫杀伤肿瘤的核心执行者,其功能状态是决定免疫治疗成败的关键。然而,由于肿瘤微环境的抑制性和T细胞免疫应答的高度异质性,免疫治疗的临床效果还不理想,患者之间、甚至同一患者的不同病灶间的免疫应答存在巨大差异。因此,精准评估内源性T细胞的免疫应答状态,对于预测免疫治疗效果、优化个体化治疗方案等都具至关重要。
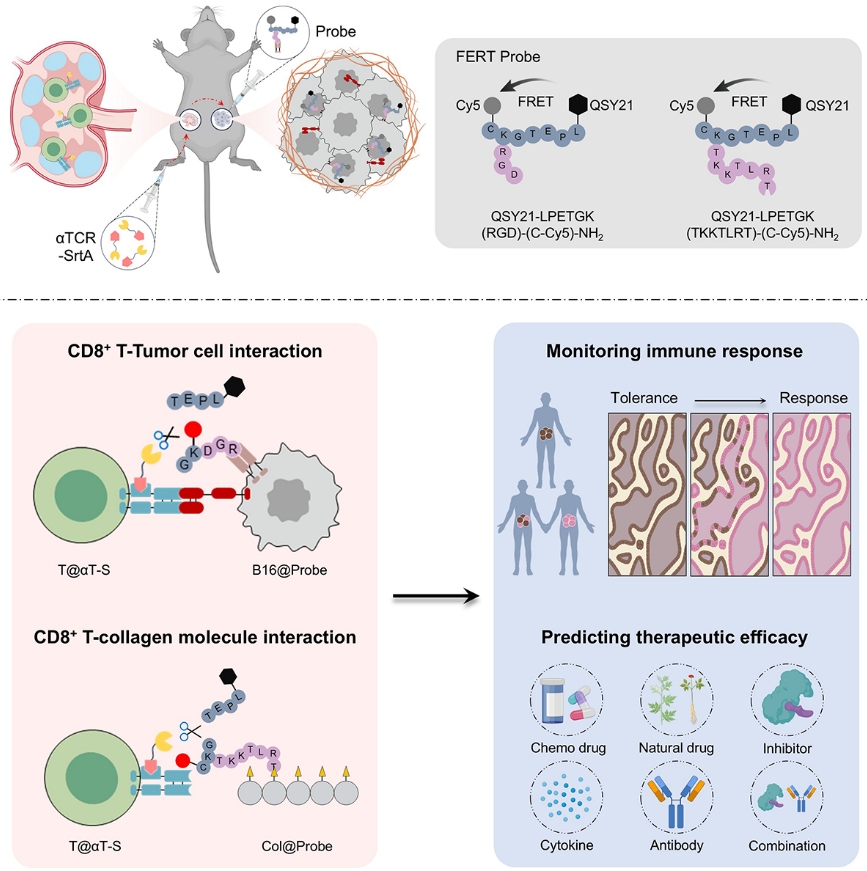
T细胞与肿瘤微环境组分的特异性互作直接决定T细胞的肿瘤杀伤效能,因此解析瘤内T细胞与其他组分的互作是精准评估T细胞免疫响应的重要措施。基于此,作者首先构建表达了抗TCR单链抗体(αTCR)与SrtA的融合蛋白(αTCR-SrtA)。该融合蛋白经小鼠脚垫注射后,可特异性结合淋巴结内的CD8⁺ T细胞,并保留SrtA对LPETG底物肽的切割活性(T@T-S细胞)。同时,基于荧光共振能量转移(FRET)原理,作者设计并合成了两种探针:QSY21-LPETGK(RGD)-(C-Cy5)-NH2与QSY21-LPETGK(TKKTLRT)-(C-Cy5)-NH2。经瘤内注射后,探针分别借助RGD肽或TKKTLRT肽特异性靶向肿瘤细胞(B16@RGD-Probe细胞)或胶原分子(Col-I@TKKTLRT-Probe分子)。当T@T-S细胞迁移至肿瘤微环境,并与B16@RGD-Probe细胞或Col-I@TKKTLRT-Probe分子发生相互作用时,T@T-S细胞表面的SrtA可高效、特异性地切割探针上的LPETG基序。这一切割效应解除了FRET效应,促使Cy5荧光恢复,从而实现对细胞间或细胞与分子间相互作用的动态示踪。该研究建立的体内临近标记系统为解析肿瘤免疫微环境中T细胞介导的免疫应答提供了新方法,并为免疫调节药物的抗肿瘤效果评价以及新型药物研发提供了有力工具。
北京大学药学院天然药物及仿生药物全国重点实验室谢海燕教授和北京理工大学生命学院聂伟东副教授为本文的通讯作者。北京理工大学博士生何佳奇为论文的第一作者。该研究获得国家自然科学杰出青年基金、国家自然科学重大项目等项目的支持。
论文链接:https://doi.org/10.1016/j.celbio.2026.100454
作者简介:

谢海燕,北京大学博雅特聘教授,博士生导师,国家自然科学杰出青年基金、优秀青年科学基金获得者,教育部“新世纪优秀人才支持计划”和北京市“优秀人才资助计划”入选者,中国生物材料学会理事,中国生物工程学会生物传感、生物芯片与纳米生物技术(BBN)分会副主任委员、中国分析测试协会分析药学分会副主任委员,Smart Molecules编委,New Journal of Chemistry顾问委员。先后主持国家自然科学重大项目课题、国家重大科学研究计划(973)项目课题等科研项目16项。在Nat. Biomed. Eng., Cell. Rep. Med., Cell Biomater., Sci. Adv., Nat. Common., J. Am. Chem. Soc., Angew. Chem. Int. Edit.等刊物发表SCI收录论文117篇;申请国家发明专利14项,并已授权转化2项,其中1项已投入大批量生产;获省部级自然科学一等奖1项、技术发明特等奖1项。