
2019年9月11日,我室邓宏魁研究团队、解放军总医院第五医学中心陈虎研究团队及首都医科大学附属北京佑安医院吴昊研究团队合作在《新英格兰医学杂志》(The New England Journal of Medicine)发表了题为《利用CRISPR基因编辑的成体造血干细胞在患有艾滋病合并急性淋巴细胞白血病患者中的长期重建》(CRISPR-Edited Stem Cells in a Patient with HIV and Acute Lymphocytic Leukemia)的研究论文,建立了基于CRISPR在人成体造血干细胞上进行CCR5基因编辑的技术体系,实现了经基因编辑后的成体造血干细胞在人体内长期稳定的造血系统重建。在成体造血干细胞上的基因编辑并不会对其他组织器官及生殖系统产生影响。该工作初步证明了基因编辑的成体造血干细胞移植的可行性和在人体内的安全性,将会促进和推动基因编辑技术在临床应用领域的发展。
自二十世纪八十年代以来,艾滋病造成了重大的公共卫生问题和社会问题。1996年,艾滋病领域研究取得了里程碑式进展,HIV入侵T细胞的主要共受体CCR5被发现(邓宏魁教授是主要发现者之一)。随后的研究发现,CCR5基因呈缺陷型(CCR5-Δ32)的人群不会被R5嗜性HIV病毒感染。2007年,一名同时患有白血病和艾滋病的“柏林病人”在接受具有CCR5-Δ32突变的造血干细胞移植后,血清中的HIV病毒得到有效清除,实现了艾滋病的“功能性治愈”。因此,通过基因编辑敲除成体造血干细胞上CCR5基因,再将编辑后的细胞移植到艾滋病患者体内有可能成为“功能性治愈”艾滋病的新策略。
如何在造血干细胞中进行高效基因编辑一直是该领域实现临床应用的关键瓶颈。2017年,邓宏魁研究团队建立了利用CRISPR/Cas9进行人造血干细胞基因编辑的技术体系。经过基因编辑后的人造血干细胞在动物模型中长期稳定地重建人的造血系统,其产生的外周血细胞具有抵御HIV感染的能力,该研究成果发表在《Molecular Therapy》杂志。为了实现该技术在临床上的应用,在此基础上进行了一系列的优化:1)建立了能进行基因编辑造血干细胞的预处理培养方法;2)通过非病毒转染的方式将Cas9-gRNA核糖核蛋白复合体递送进细胞,规避了外源DNA的引入;3)缩短了Cas9在细胞内的持续时间,从而极大的降低了脱靶效应;4)引入了配对的gRNA策略,并对使用的gRNA进行了截短及修饰,在提高基因编辑效率的同时也降低脱靶效率。
基于此优化技术体系,在通过原解放军第307医院伦理委员会审批后,该研究团队进行了ClinicalTrials.gov网站上临床研究注册(NCT03164135)。研究团队将CCR5敲除后的供者来源的CD34+成体造血干细胞回输到患有白血病合并艾滋病的患者体内,进行了长达两年的移植重建及基因编辑效果的评价。研究结果发现:1)在供者来源的CD34+细胞上实现了17.8%的CCR5基因敲除效率;2)移植后4周,患者白血病处于完全缓解状态,供者型骨髓细胞嵌合率达100%;3)经过长达19个月的随访发现,患者白血病处于持续完全缓解状态,供者型细胞完全嵌合,骨髓细胞中能够持续检测到CCR5基因编辑;4)为了初步探索治疗的有效性,对该患者短暂停止服用抗HIV病毒药物。在短暂停药期间,CCR5基因编辑的T细胞表现出一定程度抵御HIV感染的能力;5)19个月的观察中并未发现基因编辑造成的脱靶及其他副作用。这些结果表明,基于CRISPR的成体造血干细胞基因编辑技术能够在患者体内实现长期稳定的基因编辑效果,经过编辑后的成体造血干细胞能够长期重建人的造血系统。
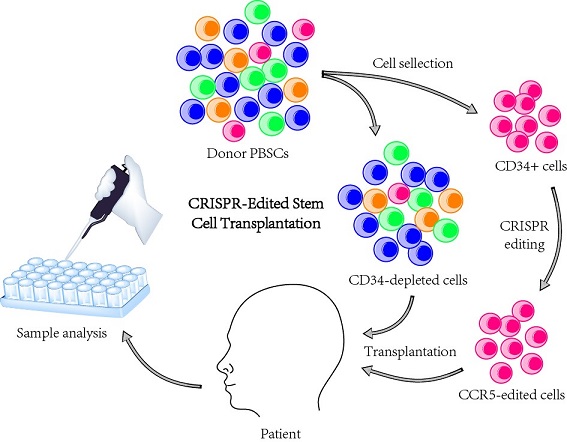
基因编辑的造血干细胞移植流程图
在成体造血干细胞上的基因编辑只局限在造血干细胞及其分化产生的血细胞中,而不会对其他组织器官及生殖系统产生影响。以CRISPR为代表的基因编辑技术在疾病的治疗上具有极大的应用潜力,有望为艾滋病、镰刀型贫血、血友病、β地中海贫血等血液系统相关疾病的治疗带来新的曙光。本研究针对基因编辑安全性和有效性进行了一系列的优化,首次在人体内探索了基因编辑的造血干细胞移植的可行性和安全性,对于推动基因编辑技术治疗多种疾病的临床研究具有重要参考价值。在今后的研究中,进一步提高基因编辑效率及优化移植方案,有望加速基因编辑造血干细胞移植技术向临床疾病治疗转化进程。
本工作获得了北京市科学技术委员会基金及天然药物及仿生药物国家重点实验室等基金的大力支持。北京大学邓宏魁教授,解放军总医院第五医学中心陈虎教授及北京佑安医院吴昊教授为该论文的共同通讯作者。徐磊博士、王军博士、博士生刘宇林及谢良福为该论文的共同第一作者。北京大学李程教授,博士生王龙腾为该研究做出了重要贡献。陈虎教授是全国造血干细胞移植领域的领军人物,在该研究中起到了关键作用。不幸的是,陈虎教授于2019年7月24日因病逝世,这项工作的发表也是对陈虎教授最真挚的缅怀!
原文链接:https://www.nejm.org/doi/full/10.1056/NEJMoa1817426?query=featured_home
(编辑:宋书香)