2022年,我室屠鹏飞/曾克武团队连续在中药化学生物学领域取得重要成果,在ACS Central Science(IF=18.728)、ACS Nano(IF=18.027)、Small(IF=15.153)、Science Advances(IF=14.957)、Acta Pharmaceutica Sinica B(IF=14.903)、eBiomedicine(IF=11.205)、Pharmacological Research*2(IF=10.334)等国际权威学术杂志上发表了一系列研究论文,简要回顾如下。
1. 揭示中药瓜蒂活性成分葫芦素B的抗肿瘤靶点及生物学功能
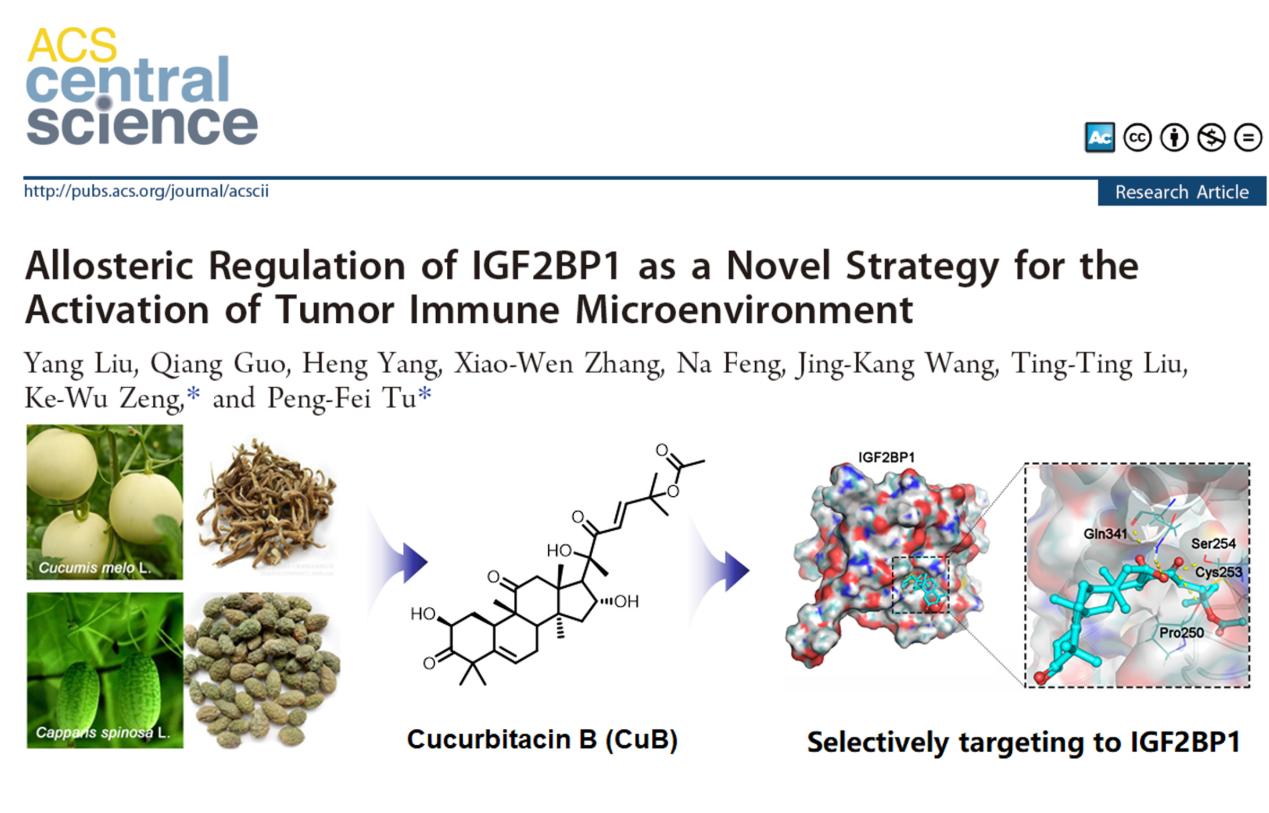
葫芦素B (Cucurbatacin B, CuB) 是瓜蒂等葫芦科清热解毒中药的主要药效成分,以葫芦素B为主要成分的葫芦素制剂在临床上广泛用于湿热毒盛所致的迁延性肝炎、肝硬化和原发性肝癌的治疗。但葫芦素B抗肝癌的直接作用靶点至今尚未明确,影响其作用机制的深入阐释和临床精准用药。团队利用前期建立的靶点“钩钓”技术平台,通过构建葫芦素B活性分子探针,揭示了其直接作用靶蛋白为—IGF2BP1。进一步研究发现,葫芦素B通过共价结合IGF2BP1的KH结构域的253位半胱氨酸残基,诱导靶点蛋白变构,阻断其对下游m6A靶基因的识别并发挥抗肿瘤及改善肿瘤免疫微环境的作用。该研究成果为肿瘤的免疫治疗提供了中医药特色的全新药理靶点,并为创新药物的设计提供了新思路。
该论文发表于ACS Central Science,药学院2017级博士刘扬为论文的第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员和屠鹏飞教授为论文的共同通讯作者。
2. 揭示中药野马追活性成分野马追内酯B的抗神经炎靶点及生物学功能

野马追内酯B(Eupalinolide B,EB)是传统药用植物野马追的代表性活性成分,具有显著的抗神经炎症活性,为了揭示EB的直接作用靶点,该研究构建了生物素修饰的EB分子探针,利用人类蛋白质组芯片筛选出EB发挥抗神经炎症作用的靶点——去泛素化酶7(USP7)。机制研究发现,EB通过诱导USP7 HUBL区的构象变化,导致USP7处于“Over-open”的失活状态,从而引发底物蛋白Keap1的降解和Nrf2抗炎信号通路的激活。此外EB还能通过抗神经炎症显著提高痴呆小鼠的学习记忆能力及改善帕金森病小鼠的动作协调性,显示出了对老年性痴呆及帕金森病的治疗效果。
该论文发表于Science Advances,药学院2020级博士生张晓雯和博士后冯娜为论文的共同第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员和屠鹏飞教授为论文的共同通讯作者。
3. 揭示中药蟾酥活性成分蟾毒灵的抗肿瘤靶点及生物学功能
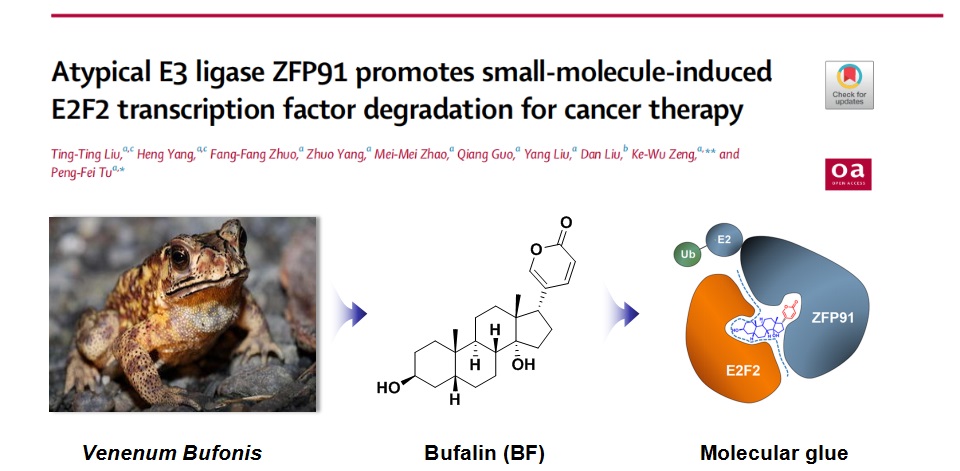
蟾毒灵(Bufalin,BF)是传统中药蟾酥的代表性抗肿瘤活性成分。为了揭示蟾毒灵的直接作用靶点,本团队设计了一种蟾毒灵分子探针,基于人类蛋白质组微阵列“钩钓”到其直接作用靶点为转录因子E2F2。机制研究发现,蟾毒灵能够作为分子胶水促进转录因子E2F2与非典型泛素连接酶ZFP91形成三元复合物,进而促进E2F2的泛素化和蛋白酶体途径降解,最终发挥抗肝癌的作用。该研究揭示了蟾毒灵作为天然“分子胶水”发挥抗肿瘤作用的独特药理机制,同时也为抗肿瘤药物的设计提供了具有中医药特色的新颖靶点与先导药物分子。
该论文发表于eBioMedicine,药学院博士后刘婷婷和2018级博士阳衡为论文的共同第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员和屠鹏飞教授为论文的共同通讯作者。
4. 揭示中药五味子活性成分五味子醇甲的神经保护靶点及生物学功能

五味子醇甲(Schisandrol A,SolA)是著名中药五味子的代表性药效成分,其神经保护作用最为显著,具有很大的开发潜力。该研究以五味子醇甲为分子探针,从神经细胞中“钩钓”到直接作用靶点ATP6V0d1,并发现五味子醇甲可以通过变构调控ATP6V0d1,显著激活神经细胞中的溶酶体V-ATPase活力,进而促进溶酶体酸化,最终降解凋亡相关蛋白并发挥神经细胞保护作用。该研究为新型神经保护药物的发现提供了具有中医药特色的新颖靶点及先导药物分子。
该论文发表于Acta Pharmaceutica Sinica B,药学院2019级硕士生周小清、2016级博士生赵少阳、博士后刘婷婷为论文的共同第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员为论文的通讯作者。
5. 揭示中药苏木活性成分巴西苏木素的神经保护靶点及生物学功能
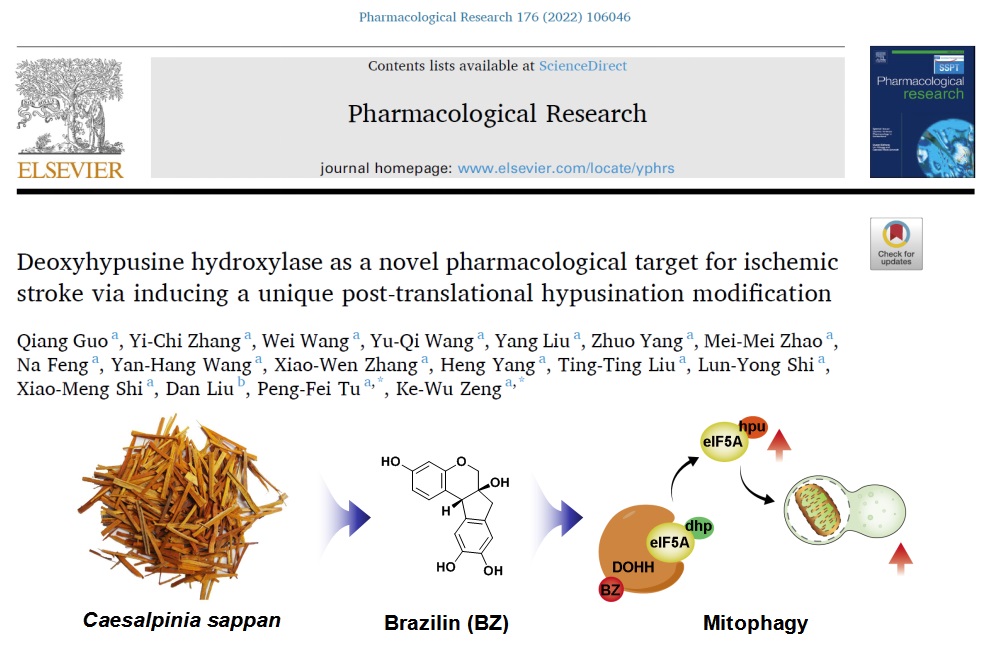
巴西苏木素(Brazilin, BZ)是传统中药苏木的代表性药效成分,具有抗缺血性脑卒中的显著疗效,但是其作用靶点和机制并不清楚。该研究通过构建巴西苏木素分子探针,利用人类蛋白质组芯片鉴定到巴西苏木素的直接作用靶点为DOHH,进而揭示了巴西苏木素通过直接作用于DOHH蛋白的Cys232后变构激活DOHH,增加eIF5A hypusine翻译后修饰,提高线粒体自噬水平,进而发挥神经保护作用的分子机制。该研究为抗缺血性脑卒中的创新药物发现提供了新颖靶点及先导药物分子。
该论文发表于Pharmacological Research,药学院博士后郭强(现就职于首都医科大学中医药学院)为论文第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员和屠鹏飞教授为论文的共同通讯作者。
6. 揭示天然活性成分环氧木香内酯的抗神经炎靶点
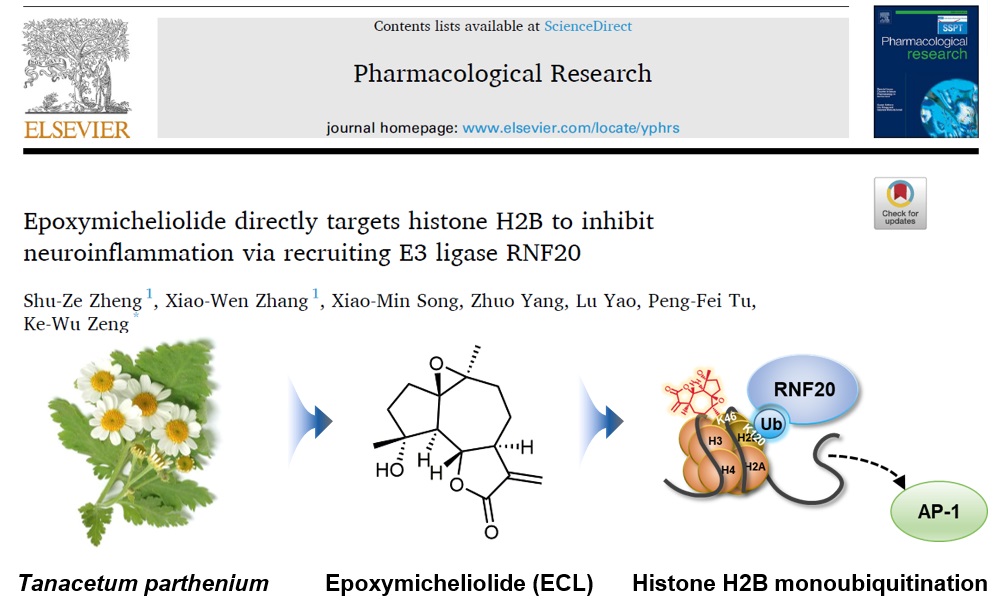
环氧木香内酯(Epoxymicheliolide, ECL)是来源于小白菊中具有抗炎的倍半萜内酯化合物。该研究制备了ECL光交联亲和介质芯片,利用SPRi高通量筛选到ECL的直接作用靶点为组蛋白H2B。ECL通过共价修饰H2B K46,从而招募E3 泛素连接酶RNF20,催化H2B的120位赖氨酸发生单泛素化,进而破坏AP-1介导的促炎信号激活,发挥抗神经炎症作用。该研究揭示了组蛋白H2B K46这一全新的抗炎靶点,为治疗神经炎症的创新药物发现提供了新的研究思路。
该论文发表于Pharmacological Research,药学院2019级硕士生郑舒泽和2020级博士生张晓雯为论文的共同第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员为论文的通讯作者。
7. 揭示天然活性分子咖啡酸碳量子点的抗肿瘤机制

长期以来,关于天然产物的研究大多聚焦于单体分子的生物学活性,而很多天然单体分子会在药材炮制及食品加工过程的高温中形成纳米物质,特别是碳量子点,进而发挥其独特的生物学效应。该研究制备了一种基于天然产物绿原酸(Chlorogenic acid, ChA)的碳量子点,其可以发挥类谷胱甘肽GSH氧化酶的活性,进而诱导肿瘤细胞内氧化还原体系失衡,表现出显著的诱导细胞铁死亡的作用。特别是绿原酸碳量子点还具有激活肿瘤免疫微环境,并将冷肿瘤转换成热肿瘤的能力。该研究可以为基于天然产物碳量子点的创新药物发现提供新的思路。
该论文发表于ACS Nano,药学院2020级硕士生姚璐为论文的第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员和屠鹏飞教授为论文的共同通讯作者。
8. 揭示天然活性成分齐墩果酸自组装纳米颗粒的抗肿瘤机制
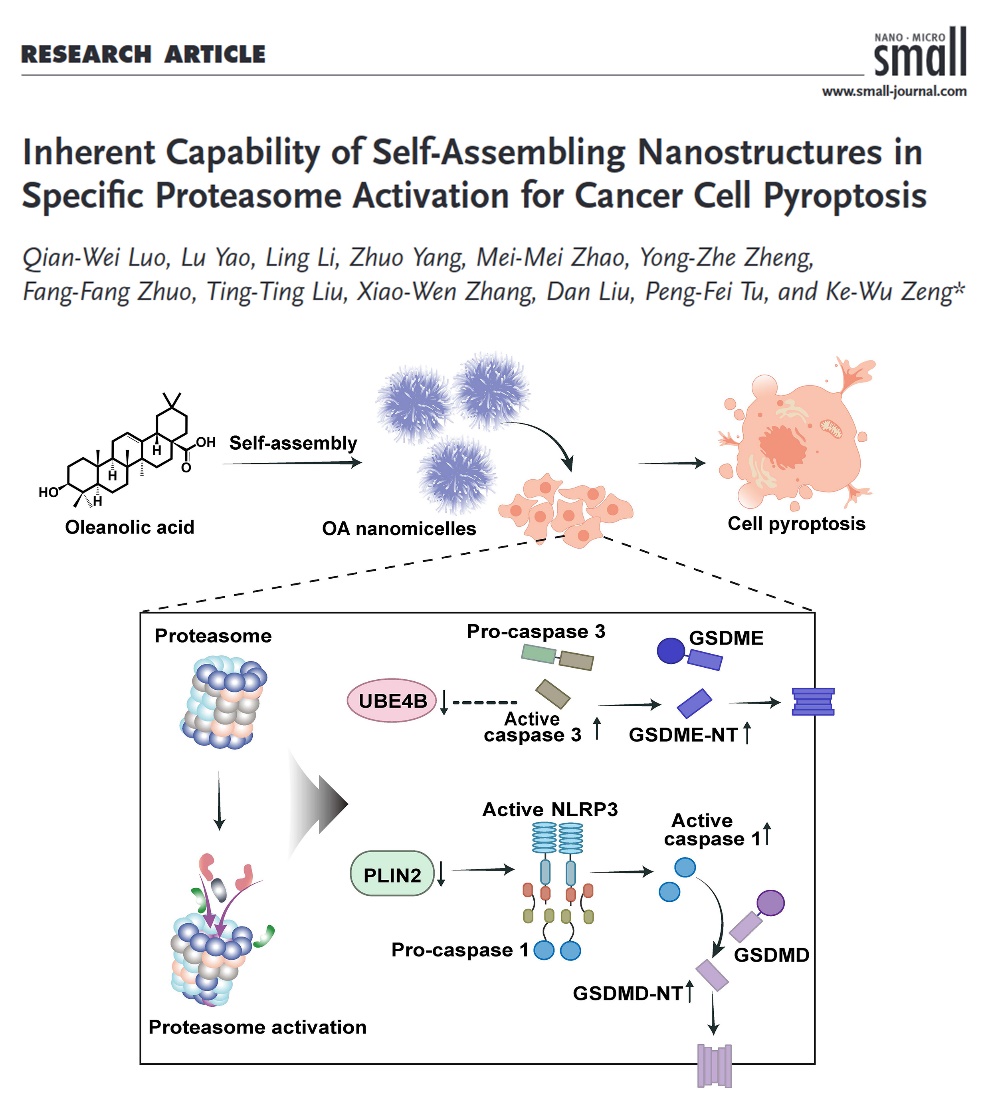
天然小分子可基于其自身特殊结构自发组装成纳米微粒。该研究发现天然产物齐墩果酸 (Oleanolic acid, OA)可以在水溶液中形成稳定的纳米胶束(OA NMs),但是其药理活性及潜在机制尚不清楚。研究发现,OA NMs在体外培养细胞模型及体内荷瘤鼠模型上均表现出显著的促进肿瘤细胞焦亡的特性。在此基础上,通过热蛋白组分析技术进一步鉴定到该纳米胶束与肿瘤细胞中的20S蛋白酶体蛋白α环亚基6(PSMA6)存在直接作用,进而导致蛋白酶体激活并诱导下游焦亡信号通路的启动。该研究揭示了天然自组装纳米胶束通过特定靶点蛋白(纳米蛋白冠)诱导肿瘤细胞焦亡的独特分子机制,同时也将人们探索天然产物的视角从单分子尺度向更大的纳米尺度拓展,为天然纳米药物的研发提供了崭新方向。
该论文发表于Small,药学院2017级长学制硕士生罗倩微为论文第一作者,北京大学天然药物及仿生药物国家重点实验室曾克武研究员为论文的通讯作者。
【通讯作者简介】

曾克武,北京大学药学院研究员,博士生导师,入选教育部高层次人才计划。长期从事天然活性分子探针的发现与药物靶点鉴定研究,以通讯/第一作者在PNAS,Sci Adv,ACS Cent Sci,ACS Nano,STTT,Small,EBioMedicine,APSB等国际学术期刊发表系列研究论文53篇,研究成果入选2017年度“中国十大医学进展”,申请发明专利11项,承担基金委、科技部、国际合作等科研课题12项,目前担任世界中医药学会联合会、中国中西医结合学会、中国药理学会等学术团体的理事、委员和青年委员等职务。

屠鹏飞,北京大学药学院教授,博士生导师,国家杰出青年基金获得者和首批岐黄学者。承担了国家和省部级项目70余项。成功创制有效部位新药2项,获得新药证书4个。以通讯作者在PNAS、Nat Comm等国际知名期刊发表论文335篇,著作19部,授权专利72项。研究成果以第一完成人获得国家科技进步奖二等奖1项,教育部和中华中医药学会等部级科技成果奖一等奖5项,并获得2016年度“全国脱贫攻坚奖创新奖”和“最美生态公益人物”、2017年度“全国创新争先奖状”和“吴阶平医药创新奖”等荣誉。
【相关文献】
1. Liu Y, Guo Q, Yang H, Zhang XW, Feng N, Wang JK, Liu TT, Zeng KW, Tu PF. (2022) Allosteric regulation of IGF2BP1 as a novel strategy for the activation of tumor immune microenvironment. ACS Cent. Sci. 8, 1102-1115.
2. Zhang XW, Feng N, Liu YC., Guo Q, Wang JK, Bai YZ, Ye XM, Yang Z, Tu PF, Zeng KW. (2022). Neuroinflammation inhibition by small-molecule targeting USP7 noncatalytic domain for neurodegenerative disease therapy. Sci. Adv. 8, eabo0789.
3. Liu TT, Yang H, Zhuo FF, Yang Z, Zhao MM, Guo Q, Liu Y, Liu D, Zeng KW, Tu PF. (2022). Atypical E3 ligase ZFP91 promotes small-molecule-induced E2F2 transcription factor degradation for cancer therapy. EBioMedicine. 86, 104353.
4. Zhou XQ, Zhao SY, Liu TT, Yao L, Zhao MM, Ye XM, Zhang XW, Guo Q, Tu PF, Zeng KW. (2022). Schisandrol A protects AGEs-induced neuronal cells death by allosterically targeting ATP6V0d1 subunit of V-ATPase. Acta Pharm. Sin. B. 12, 3843-3860.
5. Guo Q, Zhang YC, Wang W, Wang YQ, Liu Y, Yang Z, Zhao MM, Feng N, Wang YH, Zhang XW, Yang H, Liu TT, Shi LY, Shi XM, Liu D, Tu PF, Zeng KW. (2022). Deoxyhypusine hydroxylase as a novel pharmacological target for ischemic stroke via inducing a unique post-translational hypusination modification. Pharmacol. Res. 176, 106046.
6. Zheng SZ, Zhang XW, Song XM, Yang Z, Yao L, Tu PF, Zeng KW. (2022). Epoxymicheliolide directly targets histone H2B to inhibit neuroinflammation via recruiting E3 ligase RNF20. Pharmacol. Res. 177: 106093.
7. Yao L, Zhao MM, Luo QW, Zhang YC, Liu TT, Yang Z, Liao M, Tu PF, Zeng KW. (2022). Carbon quantum dots-based nanozyme from coffee induces cancer cell ferroptosis to activate antitumor immunity. ACS Nano 16, 9228-9239.
8. Luo QW, Yao L, Ling L, Yang Z, Zhao MM, Zheng YZ, Zhuo FF, Liu TT, Liu D, Zhang XW, Liu D, Tu PF, Zeng KW. (2022). Inherent capability of self-assembling nanostructures in specific proteasome activation for cancer cell pyroptosis. Small e2205531.
(编辑:宋书香)