
2021年10月13日,我室刘涛研究员团队在国际著名期刊Molecular Cell(IF=17.970)发表了最新研究成果 “Improving the efficiency of CRISPR-Cas12a based genome editing with site-specific covalent Cas12a-crRNA conjugates” 。
CRISPR技术自报道以来发展迅速,被广泛应用于哺乳动物细胞的基因组编辑与基因调控,在基因遗传病的治疗中展现出巨大的发展潜力。CRISPR/Cas12a相较于目前最为常用的CRISPR/Cas9系统具有更低的脱靶率和不同的识别序列,是一种更为精确的基因编辑系统,有望为临床治疗提供更为安全的基因编辑工具。然而,由于Cas12a系统的基因编辑效率较低,严重限制了其发展应用。因此改善Cas12a系统的基因组编辑效率,是一个亟待解决的科学问题。CRISPR/Cas12a编辑系统由蛋白质和核酸两个部分组成:核酸酶Cas12a蛋白负责切割基因组DNA,向导RNA(crRNA)则通过碱基互补配对的方式引导核酸酶到指定基因组位点进行切割。针对这一科学问题,刘涛研究员团队从化学的视角理解基因编辑事件,并提出蛋白质核酸共价偶联复合物的策略,既通过生物正交反应实现Cas12a与crRNA的共价交联,从而将基因编辑中Cas12a、crRNA与基因组DNA之间的三分子反应转化为两分子反应,来实现编辑效率的提升。
蛋白质核酸共价偶联复合物的核心难题在于如何实现Cas12a和crRNA的偶联而不影响复合物的功能,基于这一问题,刘涛团队采用基因密码子扩展技术在Cas12a核酸酶上定点引入了含有叠氮基团的非天然氨基酸,进而与5’端修饰DBCO的crRNA共价偶连。试验表明,该共价偶联策略,在不同类型细胞中都显著的提高了Cas12a系统的基因编辑效率,且不会产生额外的脱靶效应。在此基础上,作者将该技术应用于CAR-T细胞的高效制备从而显著提高Cas12a系统的基因编辑效率,并将其应用于定点整合CAR-T细胞及通用型CAR-T细胞的制备(如图),有望推动新一代更安全可控的免疫细胞制备。该研究为Cas12a系统的广泛使用奠定了基础,并为其他低效的Cas核酸酶改造提供了思路与方法。
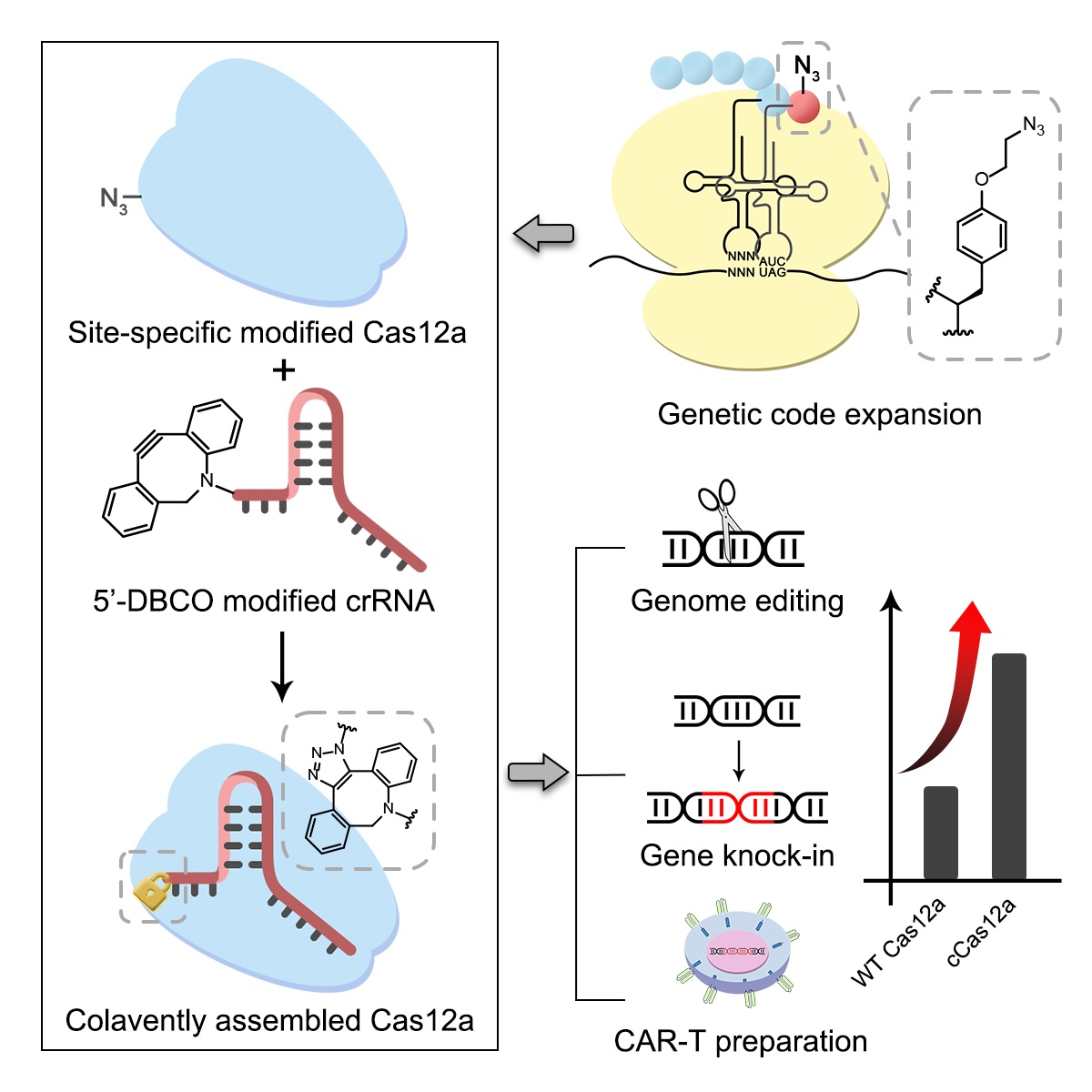
定点修饰Cas12a偶连crRNA提高Cas12a系统基因组编辑效率
北京大学药学院刘涛研究员为该工作的通讯作者,刘涛团队19级博士研究生凌鑫宇及20级博士研究生常丽颖为该论文的共同第一作者,北京大学天然药物及仿生药物国家重点实验室为第一责任通讯单位。该工作获得了国家自然科学基金(91853111, 21778005和21922701)、北京市自然科学基金项目(JQ20034)、国家重大新药创制专项(2019ZX09739001)、深圳市合成生物学研究所科研计划(DWKF20190004)、临床医学+ X青年学者计划(PKU2020LCXQ029)、北京大学医学部优秀博士研究生创新基金(71006Y2460)的资助。

左起:常丽颖(20级博士研究生),刘涛(研究员),凌鑫宇(19级博士研究生)
论文链接:https://www.sciencedirect.com/science/article/pii/S1097276521007735
【作者简介】

刘涛,北京大学药学院特聘研究员,博士生导师,分子与细胞药理学系主任,天然药物及仿生药物国家重点实验室独立PI。国家优青,北京市杰青获得者。在Nat Chem Biol, Science Advances, J Am Chem Soc, Angewandte Chemie, Cell Chem Biol等国际顶级期刊发表科研论文30余篇。团队研究方向包括生物技术在生物药物研发以及疾病机理解析中的应用。发展了含有人造氨基酸的蛋白创新药物,应用在肿瘤及基因治疗等多种领域,从而促进了生物药物的升级换代。