2025年5月7日,我室王晶教授联合中国科学院遗传与发育生物学研究所武照伐研究员及北京大学生命科学学院李毓龙教授在Nature Communications杂志上发表题为“A high-performance fluorescent sensor spatiotemporally reveals cell-type specific regulation of intracellular adenosine in vivo”的文章,该研究成功开发了首个用于检测胞内腺苷的基因编码荧光探针HypnoS(Hypersensitive intracellular adenosine Sensor),并借助多种活体成像前沿手段,深入探究了活体动物中胞内腺苷在时空动态上的细胞特异性调控,并解析了腺苷稳态的复杂分子调控过程。

腺苷(Adenosine,Ado)是一种重要的神经调控分子,在神经可塑性、运动功能、学习记忆及睡眠调节等多个生理过程中发挥重要作用。此外,腺苷作为一种代谢分子,与细胞内的能量平衡密切相关。越来越多的证据表明,腺苷信号及腺苷代谢参与癫痫、卒中、神经退行性疾病等多种中枢神经系统疾病的病理过程。解析大脑内腺苷的生成、释放及其动态调控机制,对于理解其在生理和病理中的作用至关重要。Ado在胞外的浓度受多种生物过程调节,包括胞外ATP降解生成胞外腺苷(extracellular adenosine, eAdo),以及胞内腺苷(intracellular adenosine, iAdo)经由平衡核苷转运体ENT1/2转运至胞外。腺苷的细胞来源、释放机制以及跨膜转运的具体过程仍存在诸多争议。当前研究领域面临的核心挑战之一是如何明确腺苷的具体来源及多种途径对生理或病理过程的贡献。
HypnoS是一个全新的基因编码荧光探针,由循环重排绿色荧光蛋白(cpEGFP)与腺苷脱氨酶(PvADA)融合构建而成(图1)。HypnoS具备极高的灵敏度(响应幅度>900%)、适宜的亲和力(EC50 ~11 μM)、亚秒级动力学特性及良好的选择性,重要的是HypnoS表达对神经元的正常生理过程无明显影响,这些特性使其成为检测生理和病理条件下胞内腺苷变化的理想工具。在细胞水平上,脑中不同的类型细胞对胞内腺苷(iAdo)生成、代谢及释放的差异仍不明确,胞外腺苷(eAdo)来源于神经元还是相邻的胶质细胞在领域内存在争议。利用新型HypnoS的可遗传编码特性,作者将HypnoS探针分辨表达在了神经元及星形胶质细胞,在原代培养的细胞、急性脑片以及自由活动小鼠等多种体系中实现了对iAdo动态的细胞特异性监测(图1)。研究发现神经元和星形胶质细胞腺苷的水平、动力学及释放存在显著差异,提示两种细胞类型对腺苷稳态的不同贡献。

图1 HypnoS的设计、表征及应用
利用新型HypnoS探针结合在体大视场成像,作者首次在活体小鼠整个大脑皮层尺度可视化了急性癫痫发作期间iAdo的动态变化。研究发现iAdo变化显著滞后于癫痫引发的神经元钙活动并持续更长时间,这与iAdo在癫痫发作后的潜在神经保护作用一致(图2a-b)。进一步地,作者运用活体双光子成像技术,在单细胞水平解析了iAdo在神经元及星形胶质细胞中的动态变化,并发现星形胶质细胞能够以更快的速度降解iAdo,这一发现拓展了不同细胞对癫痫期间腺苷代谢调控机制的理解(图2c-g)。
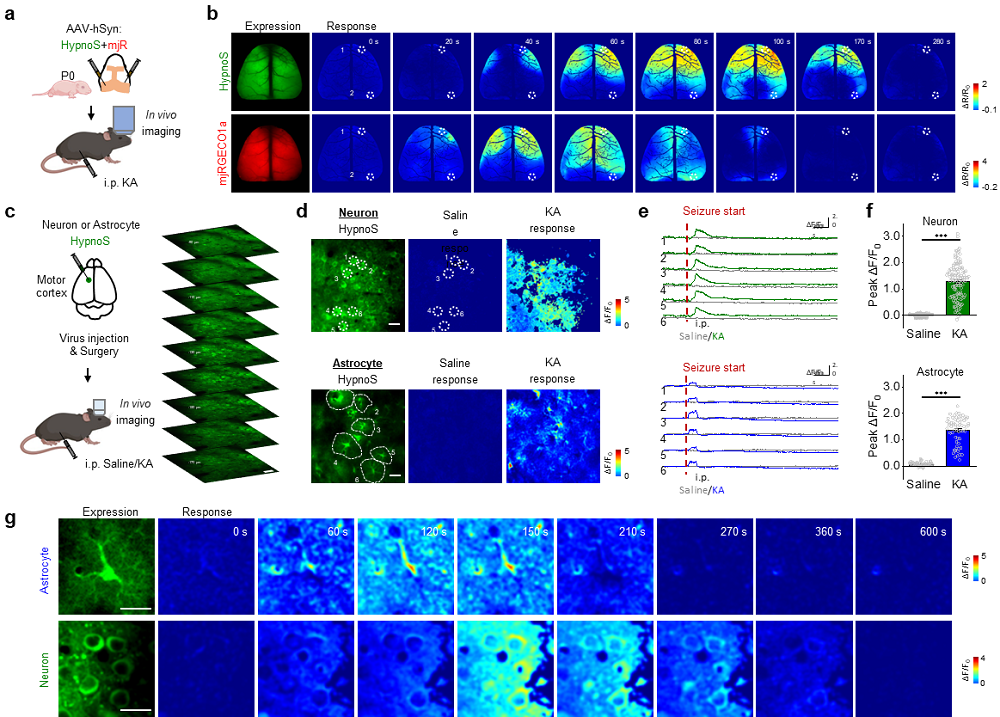
图2 HypnoS检测癫痫发作过程中胞内腺苷的动态变化。a-b, 小鼠癫痫发作过程HypnoS与钙探针mjRGECO1a的大视场成像。c, 实验示意图,显示在小鼠运动皮层进行活体双光子成像以研究癫痫期间神经元和星形胶质细胞胞内腺苷动态。d-g, HypnoS检测小鼠癫痫发作过程中神经元与星形胶质细胞胞内腺苷动态差异。
在生理过程中,腺苷被认为是调控睡眠稳态的重要分子,其作用机制长期受到关注。利用新型HypnoS探针,作者在基底前脑(BF)记录了iAdo在睡眠-觉醒周期中的变化,发现其在清醒和快速眼动(REM)睡眠期间升高,而在非快速眼动(NREM)睡眠期间降低(图3)。进一步研究表明,这些变化受ENT1/2调控且同样具有细胞特异性(图3)。这一发现提示神经元与星形胶质细胞在睡眠-觉醒过程中对于腺苷转运调控的不同模式:神经元中的ENT1/2在主要介导iAdo的释放,而星形胶质细胞中则促进腺苷的摄取。
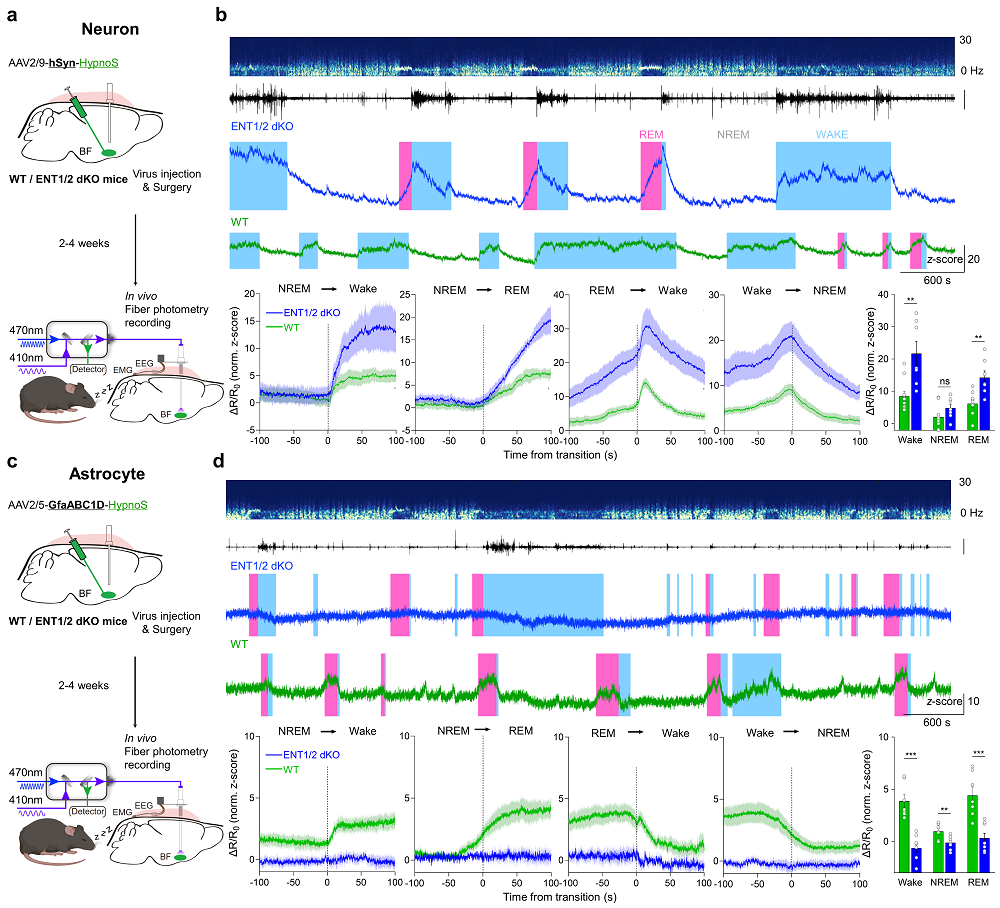
图3 睡眠-觉醒周期中胞内腺苷的动态及细胞特异性调控。a-b,睡眠-觉醒周期中ENT1/2 介导的腺苷转运在神经元中的作用。c-d, 睡眠-觉醒周期中ENT1/2 介导的腺苷转运在星形胶质细胞中的作用。
综上,该研究开发了全新的胞内腺苷荧光探针HypnoS,首次在活体动物中探究了生理及病理过程中胞内腺苷的细胞特异性时空动态,并在神经元及星形胶质细胞中可视化的检测了ENT1/2介导的腺苷跨膜转运。由于腺苷代谢及其信号传递参与多种生理(睡眠-觉醒调控等)及病理过程(癫痫、中风、神经退行性疾病及肿瘤免疫等),这项工作为理解腺苷的作用机制提供了全新工具。
北京大学药学院博士生魏庆鹏、中国科学院遗传与发育生物学研究所博士生白泽枭、北京大学生命科学学院博士生王蕾为该论文的共同第一作者。北京大学药学院王晶研究员、中国科学院遗传与发育生物学研究所武照伐研究员、北京大学生命科学学院李毓龙教授为共同通讯作者。王晶(北京朝阳医院)、王艺潘等也做出了重要贡献。论文的合作者还包括深圳理工大学的助理教授周鹏程博士等,该研究得到了北京大学天然药物及仿生药物全国重点实验室和膜生物学全国重点实验室、中国科学院分子发育生物学国家重点实验室、国家自然科学基金、科技部和北京市科协“青年人才托举工程”等机构、经费和项目的大力支持。
论文链接:https://www.nature.com/articles/s41467-025-59530-7
【作者简介】

魏庆鹏,北京大学药学院化学生物学系2021级博士研究生,研究方向为基于可遗传编码荧光探针的生物成像技术开发。目前以第一作者或共同第一作者身份在Nat. Commun.、Angew. Chem. Int. Ed.、ACS Sen.等杂志上发表多篇学术论文。

王晶,长聘副教授,研究员(PI),博士生导师,北京大学化学生物学系副主任。2016年加入北京大学药学院化学生物学系,天然药物及仿生药物全国重点实验室PI,北京大学国家生物医学成像科学中心PI(兼)。目前担任中国药理学会分析药理学专业委员会委员和青年委员会常委。课题组聚焦开发高特异性、高灵敏度和高时空分辨率的化学生物学技术(化学标记、组学、探针和成像技术)实现细胞信号分子动态的精准检测和分子机制研究。主要研究成果发表于Nat. Biotechnol.、Nat. Chem.、Nat. Protoc.、Nat. Commun.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.等国际权威学术期刊。获得北京大学拜耳研究员奖、北京大学医学部青年科技奖等奖励。