4月2日,张宏权教授研究团队在经典细胞生物学杂志“Journal of Cell Biology” 发表题为“Src-mediated phosphorylation converts FHL1 from tumor suppressor to tumor promoter” 的研究论文(2018, 217(4) 1335-1351; DOI:10.1083/jcb.201708064),同时,该论文被选为该期唯一的一篇“In Focus”聚焦论文,该刊科学编辑Ben Short撰写了“ Src turns FHL1 to the dark side” 聚焦报道。该研究揭示了重要蛋白激酶Src促癌作用的新机制,并颠覆性地改变了对抑癌FHL1蛋白在肿瘤发生发展中作用的传统认识。张宏权教授为该文的通讯作者,其团队的王翔及魏潇凡博士为并列第一作者。该研究工作得到军事科学院军事医学研究院叶棋浓研究员团队的协助。
FHL1蛋白属于FHL家族,含有LIM锌指蛋白结构域。FHL1通过LIM结构域介导相关转录调控因子、激酶及结构蛋白等多种蛋白质相互作用,最终影响细胞的分化与发育。FHL1蛋白在骨骼肌和心脏中高表达,与某些骨骼肌和心脏疾病相关。越来越多的研究证实FHL1在肿瘤的发生发展中起重要作用,FHL1在多种肿瘤包括乳腺癌、肺癌、肝癌及结肠癌等中表达下调。FHL1可定位于胞浆、细胞核及黏着斑,通过抑制肿瘤细胞生长与运动扮演抑癌蛋白的角色。但是近期的研究却发现FHL1 促进乳腺癌病人的放疗抵抗作用,而且FHL1的高表达与接受放疗的乳腺癌病人更差的预后相关。提示FHL1在肿瘤中的作用及分子机制比传统认识的更加复杂。
张宏权团队以往的研究发现Src在黏着斑的活性可通过与整合素结合蛋白Kindlin-2相互作用来调控。而本次研究证实FHL1被Kindlin-2募集至黏着斑,并与Kindlin-2和Src形成三聚体复合物。然而,这三个复合体形成是短暂瞬时的,因为Kindlin-2和Src会竞争性结合FHL1的第四个LIM结构域。当癌蛋白Src过度激活时,Src结合FHL1并导致FHL1蛋白第149和272位酪氨酸的磷酸化,磷酸化的FHL1随即入核。有趣的是,磷酸化的FHL1会解除野生型FHL1对肿瘤细胞的抑制作用,显著促进细胞增殖及肿瘤生长。这种对肿瘤的促进作用依赖于FHL1入核后与转录因子BCLAF1的相互作用。同时,在多种肿瘤包括肺癌和肝癌等的病人标本中,证实了磷酸化FHL1水平增强,入核增多,尽管总的FHL1蛋白量在肿瘤组织中是下降的。
而当细胞中Kindlin-2蛋白占优势或过表达Kindlin-2会阻止Src与FHL1的相互作用时,Src介导的FHL1磷酸化及其入核受到抑制。FHL1将与Kindlin-2蛋白结合并定位于黏着斑参与整合素调控的细胞粘附,从而抑制细胞生长。
该工作揭示出FHL1的蛋白质翻译后修饰在肿瘤发生发展中起重要作用,特别指出FHL1蛋白发挥抑癌还是促癌作用依赖于Kindlin-2蛋白和Src活化之间的相对比例,这将决定FHL1是维持非磷酸化状态定位于黏着斑发挥其抑癌作用,还是磷酸化入核发挥促进肿瘤生长的作用。这项工作也揭示出Src致癌作用的新机制:Src要实现其强大的促癌作用需要将原本是抑癌蛋白的FHL1转变为促癌的帮凶。
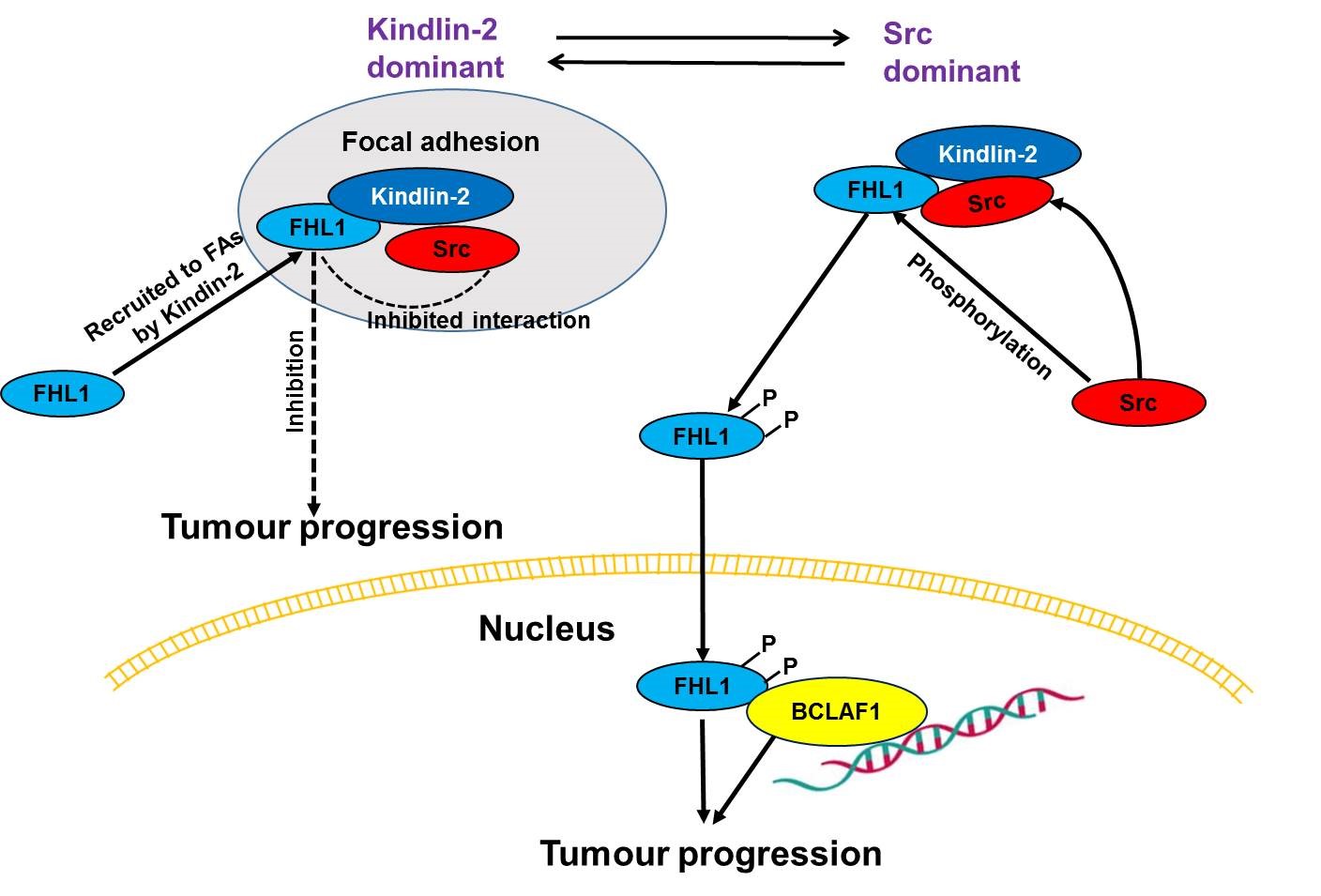
Src通过磷酸化FHL1调控肿瘤生长的新机制
该研究是张宏权教授研究团队近期在Journal of Cell Biology发表的第二篇有关整合素相关蛋白的研究工作,在上一篇报道中魏潇凡和王翔博士等解析了与FHL1相互作用的黏着斑蛋白Kindlin-2的降解机制及其对整合素激活的刹车作用。张宏权教授研究团队长期从事肿瘤细胞生物学及基质生物学领域的研究,围绕“Kindlin-2”蛋白已经发表26篇研究论文,最近还受邀在“Int J Biochem Cell Biol”发表关于Kindlins家族蛋白的专题综述“Kindlins: Roles in development and cancer progression”。
(基础医学院)
原文链接:http://sbms.bjmu.edu.cn/xyxw/195265.htm